Pinocembrine
| Pinocembrine | |
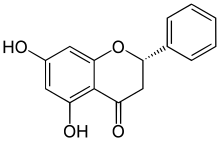 | |
| S-(+)-pinocembrine | |
| Identification | |
|---|---|
| Nom UICPA | (2S)-5,7-dihydroxy-2-phényl-2,3-dihydro-4H-chromén-4-one |
| Synonymes | dihydrochrysine |
| No CAS | 68745-38-0 (R,S-pinocembrine) 480-39-7 ((S)-(+)-pinocembrine) 206660-42-6 ((R)-(–)-pinocembrine) |
| PubChem | 238782 |
| SMILES | O=C2c3c(OC(c1ccccc1)C2)cc(O)cc3O PubChem, vue 3D |
| InChI | Std. InChI : vue 3D InChI=1S/C15H12O4/c16-10-6-11(17)15-12(18)8-13(19-14(15)7-10)9-4-2-1-3-5-9/h1-7,13,16-17H,8H2 Std. InChIKey : URFCJEUYXNAHFI-UHFFFAOYSA-N |
| Propriétés chimiques | |
| Formule | C15H12O4 [Isomères] |
| Masse molaire[1] | 256,253 4 ± 0,014 g/mol C 70,31 %, H 4,72 %, O 24,97 %, |
| Propriétés physiques | |
| T° fusion | 192-193 °C[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
modifier  | |
La pinocembrine est un composé organique de la famille des flavanones, un sous-groupe de flavonoïdes. C'est un antioxydant présent dans la damiana[3], le miel, le curcuma rond[4] et la propolis[5].
La pinocembrine peut être convertie biosynthétiquement en pinobanksine par hydroxylation du carbone adjacent à la fonction cétone. Certaines études ont montré que la pinocembrine est un médicament potentiel, entre autres dans le traitement des ischémies cérébrales, des hémorragies intracérébrales, de maladies neurodégénératives, cardiovasculaires et de l'athérosclérose[6],[7].
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Pinocembrin » (voir la liste des auteurs).
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ PubChem CID 238782
- ↑ (en) J Zhao, Dasmahapatra AK, Khan SI et Khan IA, « Anti-aromatase activity of the constituents from damiana (Turnera diffusa) », J Ethnopharmacol, vol. 120, no 3, , p. 387–393 (PMID 18948180, DOI 10.1016/j.jep.2008.09.016)
- ↑ (en) C Punvittayagul, Wongpoomchai R, Taya S et Pompimon W., « Effect of pinocembrin isolated from Boesenbergia pandurata on xenobiotic-metabolizing enzymes in rat liver. », Drug Metabolism Letters, vol. 5, no 1, , p. 1–5 (PMID 20942797, DOI 10.2174/187231211794455226)
- ↑ (en) Bosio K, Avanzini C, D’Avolio A, Ozino O et Savoia D, « In vitro activity of propolis against Streptococcus pyogenes », Letters in Applied Microbiology, vol. 31, no 2, , p. 174–177 (PMID 10972723, DOI 10.1046/j.1365-2672.2000.00785.x)
- ↑ (en) X. Lan, W. Wang, Q. Li et J. Wang, « The natural flavonoid pinocembrin: molecular targets and potential therapeutic applications », Mol Neurobiol, vol. 53, no 3, , p. 1794–801 (PMID 25744566, PMCID 4561606, DOI 10.1007/s12035-015-9125-2)
- ↑ (en) X. Lan, X. Han, Q. Li, Q. Li, Y. Gao, T. Cheng, J. Wan, W. Zhu, J. Wang, X. Lan, W. Wang, Q. Li et J. Wang, « Pinocembrin protects hemorrhagic brain primarily by inhibiting toll-like receptor 4 and reducing M1 phenotype microglia », Brain Behav Immun., vol. 61, , p. 326–339 (PMID 28007523, DOI 10.1016/j.bbi.2016.12.012)
v · m | |
|---|---|
| Flavanones |
|
| Flavanones O-méthylées |
|
| Flavanones C-méthylées | |
| Hétérosides de flavanone | |
| Flavanones acétylées |
|
| Hétérosides acétylés |
|
 Portail de la chimie
Portail de la chimie











