Methiocarb
| Methiocarb | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
 | ||||
| Algemeen | ||||
| Molecuulformule | ||||
| IUPAC-naam | 3,5-Dimethyl-4-(methylsulfanyl)phenyl N-methylcarbamaat | |||
| Andere namen | 3,5-Dimethyl-4-(methylthio)phenyl methylcarbamaat (IUPAC toegestaan) Mercaptodimethur Mesurol | |||
| Molmassa | 225,312 g/mol | |||
| SMILES | O=C(Oc1cc(c(SC)c(c1)C)C)NC | |||
| CAS-nummer | 2032-65-7 | |||
| EG-nummer | 217-991-2 | |||
| PubChem | 16248 | |||
| Wikidata | Q425378 | |||
| Beschrijving | Kleurloze kristallen | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
Neurotoxine | ||||
| Fysische eigenschappen | ||||
| Dichtheid | 1,25 g/cm³ | |||
| Smeltpunt | 118,5 °C | |||
| Kookpunt | 311°C; ontleding start bij: 300 °C | |||
| Oplosbaarheid in water | 0,027 g/L | |||
| Goed oplosbaar in | Aceton (144 g/L) Ethylacetaat 87 g/L 1-Octanol (31 g/L) Xyleen (20 g/L) | |||
| log(Pow) | 3,18 | |||
| Evenwichtsconstante(n) | KH = 1,2*10-4 Pa.m3/mol | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Methiocarb, ook bekend als mesurol[1][2] en mercaptodimethur, is een carbamaat-pesticide dat sinds de jaren zestig wordt gebruikt als vogelafweermiddel,[3] insecticide,[4] acaricide[4] en molluscicide (weekdierbestrijding)[4]. Carbamaten worden veel gebruikt in de landbouw als insecticiden en herbiciden. Zij hebben de voorkeur boven organochloorverbindingen omdat de laatste groep zeer persistent is op gewassen. Methiocarb is zowel een contactgif als een via de maag werkend gif voor mijten en het heeft een neurotoxisch effect op weekdieren, met name slakken en naaktslakken. Zaden die behandeld zijn met methiocarb zijn schadelijk voor vogels.
Chemie
Synthese
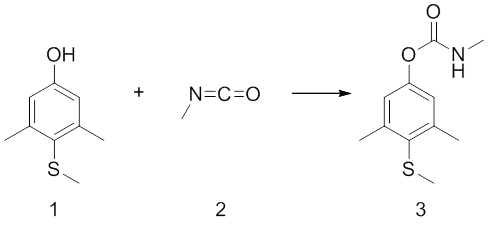
Methiocarb (3) wordt (door Bayer) gesynthetiseerd uitgaande van 4-methylthio-3,5-xylenol (1) en methylisocyanaat (2).[5] Het xylenol (1) reageert als nucleofiel (via een vrij elektronenpaar op zuurstof) met het partieel positief geladen koolstofatoom in het isocyanaat (2).
Biochemie en Farmacologie
Biochemische werking
De carbamaatfunctie in methiocarb kan door cholinesterase {CE)gesplitst worden. Dit resulteert in een carbamaat dat aan cholinesterase bindt en een aromatische alcohol.
Tijdens het splitsen van methiocarb wordt methylcarbamidezuur gevormd, dat na de reactie gebonden is aan CE. De eigenlijke functie van CE is de splitsing van de acetyl-cholinebinding. Dit resulteert in een aan CE gebonden acetylgroep. In een snelle reversibele reactie wordt de acetylgroep als azijnzuur afgestaan en CE is weer beschikbaar voor een volgende reactie.
De binding tussen CE en methylcarbamidezuur is ook reversibel, maar het afstaan van het carbamidezuur verloopt veel langzamer. Het gevolg is dat carbamidezuur de functie van CE remt met als resultaat dat de acetylcholine-concentratie veel langer op een hoge waarde blijft. In vergelijking met organofosfaten is de remming van CE door methiocarb minder. De fosfaten binden irreversibel aan CE.
Naast zijn cholinerge werking heeft methiocarb ook een endocrien verstorend effect: het heeft oestrogene, antiandrogene en aromataseremmende effecten.[6]
Metabolisme
Methiocarb wordt vooral in de lever gemetaboliseerd tot sulfoxide. Zowel methiocarb zelf als het fenol dat ontstaan is na splitsing door CE worden opdeze manier omgezet. Soms wordt het zwavel-atoom nog een keer geoxideerd, waarbij het sulfon ontstaat. Een klein gedeelte van methiocarb wordt omgezet door hydroxylering van de methylgroep aan stikstof.[7][8]
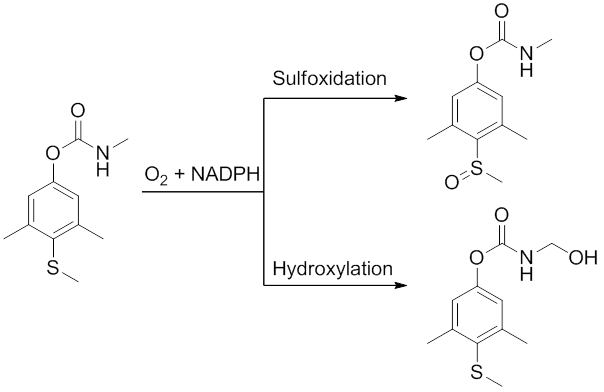
Opname van Methiocarb
Methiocarb kan op verschillende manieren het lichaam binnenkomen. Bij mensen is dit meestal via de huid of als aerosol vanwege het gebruik als pesticide in de landbouw. Voor insecten en vogels is de orale route het meest waarschijnlijk. Het NOAEL (Engels: No-observed-adverse-effect level: Niveau waarop geen negatieve effecten waarneembaar zijn) van deze routes is vastgesteld op:
- voor ratten is een orale NOAEL-waarde van 3.3 mg/kg per dag bepaald, gebaseerd op een studie van 2 jaar.
- voor konijnen is voor absorptie door de huid een NOAEL gesteld van 150 mg/kg per dag, gebaseerd op de vermindering van voedselconsumptie.[7]
- Bij ratten, gevoerd met methiocarb in een dosis van 50 ppm, wordt een verlaging van de CE-activiteit in de hersenen gevonden van 14% en 5% voor respectievelijk mannetjes en vrouwtjes.
- Ratten die worden blootgesteld aan een aerosol van 96 mg/m3 (in een oplosmiddel)) vertoonde tekenen van onwillekeurige spiercontracties (tremor). De activiteit van CE in de hersenen is verlaagd tot 61% en 74% voor respectievelijk mannetjes en vrouwtjes. Er werden geen veranderingen gemeten in de gewichten van de organen.
Op basis van de activiteit van CE in de hersenen werd de NOAEL bepaald op 6 mg/m3.[7]
Verdeling van methiocarb in het lichaam
Om de verdeling van de stof in het lichaam te bepalen is gebruik gemaakt van met koolstof-14 ([14C]) gelabeld methiocarb. Ongeveer 8 uur na een onderhuidse injectie van met [14C] gelabeld methiocarb is meer dan 20*103 dpm van de radioactiviteit aanwezig in de nieren, 14*103 dpm in de longen, 14*103 dpm in het hart, 6*103 dpm in het lichaamsvet. 26*103 dpm wordt teruggevonden in de rode bloedcellen. 30 Minuten na de injectie zijn de getallen voor alle weefsels, behalve lichaamsvet, veel hoger. Dit geeft aan dat er een snelle verwijdering van methiocarb optreedt. Daarnaast is een stijging vastgesteld in alle weefsels, met uitzondering van de rode bloedcellen, tussen 2 en 4 uur na injectie. Dit wijst erop dat na twee uur een herverdeling van de stof plaatsvindt, gevolgd door de verwijdering. In de beschreven studie is alleen naar de radioactiviteit gekeken, dus de hoeveelheid [14C]. Er is niets gezegd over de chemische aard van de stoffen waarin de radioactiviteit voorkomt. Over toxiciteit is op basis van deze studie dus weinig te zeggen.[2]
Toxiciteit
Giftigheid,korte termijn
Oraal
In een periode van 27 dagen daalde in ratten de activiteit van cholinesterase tot minder dan 50 percent ten opzichte van die bij de controlegroep. In het voedsel was 2 mg/ kg lichaamsgewicht (lg)in de eerste drie dagen en 4 mg/kg lg in de resterende 24 dagen. Er werden geen abnormale klinische verschijnselen waargenomen.[7][9]
Dermaal
Bij konijnen werd methiocarb op de huid aangebracht in hoeveelheden van 0, 60, 150 of 375 mg/kg lg per dag gedurende 6 uur/dag. De dieren uit de groep met de hoogste dosis vertoonden een verminderde voedselopname. In de groep met de hoogste dosis was de activiteit van cholinesterase na 14 en 21 dagen verlaagd bij de mannetjes, vrouwtjes vertoonden dit verschijnsel niet, onafhankelijk van de gebruikte hoeveelheid methiocarb. De activiteit van cholinesterase in erytrocyten is bij vrouwtjesratten blijkbaar, wat methiocarb betreft, niet dosis-afhankelijk [7][10]
Giftigheid, lange termijn
De langetermijngiftigheid is onderzocht een 1 jaar durende studie met 50 mannetjes en 50 vrouwtjesmuizen. De muizen hadden een dieet met 0, 15, 43 and 130 mg/kg lg per dag voor mannetjes en 0, 20, 57, and 170 mg/kg licammsgewicht lg per dag voor vrouwtjes. Voedselopname, gedrag en mortaliteit varieerden niet op basis van de verschillende doses. Na één maand was de activiteit van CE in plasma het grootst, de kleinste afname werd gemeten na 24 maanden. De activiteit in de hersenen van CE was ook verlaagd, meer bij de mannetjes dan de vrouwtjes.[7][11]
In een andere, twee jaar durende studie met 60 ratten werden diëten met 0, 3.3, 9.3 and 29 mg/kg lg per dag voor mannetjes en 0, 5, 14, and 42 mg/kg lw per dag voor vrouwtjes gebruikt. Ook hier werd noch in voedselopname, gedrag of mortaliteit enig verschil op basis van de dosis methiocarb gemeten. De CE-activiteit in plasma was vanaf de eerste dag lager.[7][12][13][14] van zowel
Milieuaspecten
Omdat methiocarb veel gebruikt wordt als insecticide op landbouwgewassen zijn ook de veiligheidsrisico's voor mensen en hun gezondheid onderzocht.
| Methiocarb | Methiocarb- sulfoxide | Methiocarb- sulfon | Hydroxy-methiocarb | Hydroxy-methiocarb-sulfoxide | Methiocarb-fenol | Methiocarb-fenol-sulfoxide | Methiocarb-fenol-sulfon | |
|---|---|---|---|---|---|---|---|---|
| Structuur formule |  |  |  |  |  |  |  |  |
| planten[15] | +++ | + | ++ | + | + | |||
| bodem[16] | 1,5 dagen | + 6 dagen | + | +++ | + 2 dagen | + 20 dagen | + | |
| water[16] | 28 dagen (pH=7) | + | + | + | ||||
| dieren | +++ | ++ | + | + | + |
Na 217 dagen waren zowel methiocarb als metabolieten niet meer aantoonbaar in bodemmonsters. In water was dat al na 32 dagen het geval.[17]
LD50 en LC50
| Blootstelling | Acute toxiciteit |
|---|---|
| Dermaal LD50 (mg/kg lichaamsgewicht) | |
| Konijn | >2000[7] |
| Rat | >200[7] |
| Inhalatie (1 hour) LC50 (mg/m3) | |
| Rat | 1200[7] |
| Intraperitoniaal LD50 (mg/kg lichaamsgewicht) | |
| Muis | 6[7] |
| Oraal LD50(mg/kg lichaamsgewicht) | |
| Hond | 10[7] |
| Cavia | 40[7] |
| Muis | 25[7] |
| Rat | 30[7] |
Werkingsbereik
Methiocarb als bestrijdingsmiddel vindt diverse toepassingen. Deze lopen uiteen van de bestrijding van lakken, insecten en knaagdieren tot het afstoten van vogels.
Insecten
Als insecticide is het effectief tegen Tripsen, een lage dosis is voor deze diertjes al dodelijk. De LC99,99 voor de concentratie in suspensies is 0.34 g/L and for the wettable powder it is 2.30, which is a bit too much for effective use.10[18]
Slakken
Voor de bestrijding van slakken is methiocarb effectief, maar in een hoge dosis. In een studie met E. vermiculata bleek methiocarb het meest effectief als het plaatselijk werd aangebracht (met DMSO als oplosmiddel). De LD50 is 414 μg per slak, de LD99,99 wordt geschat op 1400 μg per slak.[19]
Vogels
Als bescherming tegen beschadiging van fruit door vogels bleek methiocarb in een studie niet te voldoen. De stof was op vijgen gesproeid. De vogels pikten door de schil of pelden de vijgen, waardoor de blootstelling aan methiocarb laag was, en de vogels het fruit nog steeds beschadigden.[20]
In een andere studie met quelea (een groep zangvogels) werd onderzocht of metiocarb een negatief effect had op de voedselkeuze. Vastgesteld werd dat wanneer de vogels met methiocarb behandelde zaden gevoerd kregen, ze een volgende keer ander voedsel kozen. Dit toonde aan dat methiocarb effectief kan zijn als "vogelverschrikker".[21]
Knaagdieren
Verschillende onderzoeken zijn uitgevoerd naar methiocarb als rodenticide. In het eerste veldexperiment werden muizenkorrels met methiocarb over het land verspreid. Bijna 23% van de muizenpopulatie werd gedood in 1 nacht, maar het totale effect was minimaal, waarschijnlijk door migratie vanuit het omringende land. In een tweede veldstudie werden muizenkorrels met methiocarb eb muizenkorrels met strychnine met elkaar vergeleken. De methiocarb-korrels hadden ene mortaliteit van 40% tot gevolg, de strychninekorrels leidde tot 90% mortaliteit van de muizen. Hoewel methiocar in eerste instantie effectief leek, bleken de muizen snel een aversie ertegen te ontwikkelen waardoor de effectiviteit als rodenticide niet groot is.[22]
Zelfmoord door vergiftiging
Methiocarb is een gewasbeschermingsmiddel, en hoewel (een poging tot) zelfmoord met behulp van dit soort producten niet vaak voorkomt is er een geval bekend.
Een 80-jarige Duitse vrouw doodde zichzelf door het drinken van een flesje met een methiocarb-oplossing. De rozerode vloeistof zat op haar kleren, gezicht en handen (waarschijnlijk ten gevolge van braken). Ook in haar maag-darmkanaal en luchtwegen werd het aangetroffen. Het toxicologisch onderzoek toonde aan dat de opname van methiocarb niet geheel verlopen was: de concentratie methiocarb en zijn metaboieten in de urine was laag. De korte blootstelling was hiervan de oorzaak.
Hogere concentraties mehiocarb of metabolieten kunnen het gevolg zijn van post-mortemopname of herverdeling vanuit het maag-darmstelsel.
De doodsoorzaak werd vastgesteld als: dood door acute vergiftiging met methiocarb.[23]
Bronnen, noten en/of referenties
Verwijzingen in de tekst
|














