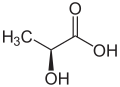
Kwas mlekowy
| ||||||||||||||||||||||||||||||||||||||||||
 Próbka kwasu mlekowego | ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | ||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | C3H6O3 | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory | C2H4OHCOOH | |||||||||||||||||||||||||||||||||||||||||
| Masa molowa | 90,08 g/mol | |||||||||||||||||||||||||||||||||||||||||
| Wygląd | enancjomery D i L tworzą kryształy[2]; racemat jest w temperaturze pokojowej bezbarwną, syropowatą cieczą[3] (poniżej temperatury topnienia tworzy żółte kryształy)[2] | |||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | ||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | 50-21-5 | |||||||||||||||||||||||||||||||||||||||||
| PubChem | 612 | |||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB04398 | |||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||
| Pochodne | ||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
Kwas mlekowy, kwas 2-hydroksypropanowy (łac. acidum lacticum), E270 – organiczny związek chemiczny z grupy hydroksykwasów, obecny w skwaśniałym mleku (skąd pochodzi jego nazwa) oraz powstający w mięśniach w trakcie intensywnego wysiłku fizycznego, kiedy dochodzi do procesu beztlenowego oddychania zwanego fermentacją mleczanową. Sole tego kwasu to mleczany.
Ze względu na to, że atom węgla, do którego przyłącza się grupa hydroksylowa, jest asymetryczny, kwas mlekowy wykazuje chiralność i ma dwa enancjomery:
- L(+) (o konfiguracji absolutnej S): kwas (S)-2-hydroksypropanowy
- D(–) (o konfiguracji absolutnej R): kwas (R)-2-hydroksypropanowy
W organizmie ludzkim występuje wyłącznie forma L(+)[6].
Kwas mlekowy w mięśniach
Powstawanie kwasu mlekowego w mięśniach jest związane z procesem spalania glukozy. W warunkach braku tlenu glikoliza jest jedynym możliwym sposobem wytworzenia energii dla komórki (ATP). Końcowymi produktami glikolizy są ATP, kwas pirogronowy oraz NADH. W celu odzyskania NAD+ atom wodoru jest przenoszony z NADH na cząsteczkę kwasu pirogronowego z wytworzeniem cząsteczki kwasu mlekowego (oddychanie beztlenowe). W warunkach tlenowych kwas mlekowy nie powstaje. Kwas pirogronowy i NADH są przenoszone do mitochondriów, gdzie w obecności tlenu są spalane do CO2 oraz H2O (wodór z NADH jest spalany, a NAD+ zwracany do cytoplazmy; oddychanie tlenowe). W obecności tlenu mitochondria mogą wykorzystywać także inne substraty niż glukoza, na przykład kwasy tłuszczowe.
Spalanie glukozy z dostatecznym udziałem tlenu:
- C
6H
12O
6 + 6O
2 → 6CO
2 + 6H
2O (z jednej cząsteczki glukozy powstają 33 cząsteczki ATP)
Spalanie glukozy przy niedoborze tlenu:
- C
6H
12O
6 → 2C
2H
4OHCOOH (z jednej cząsteczki glukozy powstają 2 cząsteczki ATP)
Wzrastające stężenie kwasu mlekowego odbiera się jako doznanie bólu w trakcie intensywnego wysiłku. Kwas ten jednak jest dość szybko odprowadzany z mięśni przez układ krwionośny, a następnie ponownie przetwarzany głównie w wątrobie do glukozy w procesie zwanym glukoneogenezą lub cyklem Corich. W zasadzie po dwóch godzinach od ustania intensywnego wysiłku fizycznego cały kwas mlekowy jest odprowadzany z mięśni. Glukoneogeneza wymaga dostarczenia energii pochodzącej z oddychania tlenowego.
Dzięki wytwarzaniu kwasu mlekowego mięsień może chwilowo osiągnąć moc przekraczającą maksymalną wydajność układu krążenia lub oddechowego, jednak gromadzenie się tego związku szybko zmusza do przerwania wysiłku. Jeśli wysiłek nie przekracza możliwości dostarczania tlenu przez ustrój, kwas mlekowy nie powstaje. Zjawisko może obejmować cały organizm albo pojedynczy mięsień.
Kwas mlekowy jest atraktantem dla komarów, co sprawia, że osoby w trakcie lub po wysiłku fizycznym są bardziej narażone na ich ukąszenia[3].
Kwas mlekowy ma znaczenie w patomechanizmie wielu chorób. Wszelkie zaburzenia oddychania tlenowego prowadzą do gromadzenia się kwasu mlekowego i kwasicy.
Zespół opóźnionego bólu mięśniowego (DOMS)
Ból mięśni występujący zwykle po 20 godzinach od wzmożonego wysiłku fizycznego, zwany czasami „zakwasem”, nie jest spowodowany kwasem mlekowym, lecz drobnymi zniszczeniami mechanicznymi w strukturze tkanki mięśniowej, powstałymi w czasie intensywnego wysiłku. Ból mięśni pojawiający się 24–72 godzin po intensywnym wysiłku nazwano zespołem opóźnionego bólu mięśniowego (DOMS, od ang. delayed-onset muscle soreness). Zespół ten został opisany po raz pierwszy w 1900 przez Theodore’a Hougha, który wysunął hipotezę, że ten rodzaj bólu jest rezultatem uszkodzeń wewnątrz mięśnia[7]. Nasilenie DOMS zależy od rodzaju wykonanego wysiłku oraz dominującego typu skurczu włókien mięśniowych.
Obecnie przyjmuje się, że DOMS powiązany jest z uszkodzeniami mięśni lub tkanki łącznej i następczą odpowiedzią zapalną niezbędną do regeneracji tkanek. Jedna z hipotez przyjmuje, że rozwinięcie stanu zapalnego wywołującego pobudzenie nocyceptorów (receptorów bólu) wymaga pewnego czasu, co tłumaczy opóźnione pojawienie się bólu[8].
Kwas mlekowy w produktach spożywczych
Kwas mlekowy powstaje w produktach spożywczych otrzymywanych przez fermentację mlekową, nadając im charakterystyczny, kwaskowy smak. Sumaryczny przebieg fermentacji mlekowej jest identyczny z procesem niekompletnego spalania glukozy w mięśniach, choć jej mechanizm jest zupełnie inny. Czasami proces spalania glukozy w mięśniach jest nazywany fermentacją mleczanową. Kwas mlekowy w produktach spożywczych jest wynikiem fermentacji cukrów – laktozy (obecnej w mleku), fruktozy (obecnej w warzywach i owocach) i innych. Obecność kwasu mlekowego w mleku powoduje koagulację białek wchodzących w jego skład, wskutek czego mleko zmienia swoją strukturę i smak. Proces ten jest masowo wykorzystywany przy produkcji serów, jogurtów, kefiru i innych produktów mlekopochodnych.
Kwas mlekowy powstaje też w wyniku celowego fermentowania niektórych warzyw, między innymi ogórków i kapusty. Jego względnie duże stężenie powoduje zmianę struktury tych warzyw (ciemnienie, mięknięcie, kurczenie się) i nadaje im charakterystyczny smak.
Zastosowanie
Znajduje zastosowanie w przemyśle garbarskim i tekstylnym. Jest używany do regulacji kwasowości w przemyśle cukierniczym, a w pszczelarstwie do zwalczania roztocza Varroa destructor.
W przemyśle chemicznym może być stosowany do otrzymywania glikolu propylenowego oraz kwasu akrylowego. Prowadzone są prace mające na celu otrzymywanie z kwasu mlekowego polimerów użytecznych (polilaktydy)[9][10], na przykład do wyrobu biodegradowalnych toreb jednorazowego użytku[11] (z polikwasu mlekowego).
Polimer kwasu mlekowego (PLA) jest powszechnie używanym filamentem w druku 3D.
Przypisy
- ↑ a b c Farmakopea Polska IX, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2011, s. 4574, ISBN 978-83-88157-77-6 .
- ↑ a b c d e f g h Haynes 2014 ↓, s. 3-336.
- ↑ a b Podręczny słownik chemiczny, RomualdR. Hassa (red.), JanuszJ. Mrzigod (red.), JanuszJ. Nowakowski (red.), Katowice: Videograf II, 2004, s. 212, ISBN 83-7183-240-0 .
- ↑ Farmakopea Polska VI, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2002, s. 1176, ISBN 83-88157-18-3 .
- ↑ Haynes 2014 ↓, s. 5-95.
- ↑ AleksanderA. Chmiel AleksanderA., Biotechnologia. Podstawy mikrobiologiczne i biochemiczne, Warszawa: Wydawnictwo Naukowe PWN, 1991, s. 75, ISBN 83-01-10320-5 .
- ↑ TheodoreT. Hough TheodoreT., Ergographic studies in muscular soreness, „Journal of the Boston Society of Medical Sciences”, 5 (3), 1902, s. 81–92, PMID: 19971340, PMCID: PMC2048417 .
- ↑ Muscle Soreness and Damage and the Repeated-Bout Effect, [w:] KenK. Nosaka KenK., Skeletal Muscle Damage and Repair, Human Kinetics, 2008, s. 63–64, ISBN 978-0-7360-5867-4 .
- ↑ ElizabethE. Royte ElizabethE., Corn Plastic to the Rescue [online], Smithsonian, 2006 [dostęp 2009-05-13] (ang.).
- ↑ NaturePlus Home Compostable Starch-Based Film [online], Amcor Limited [dostęp 2009-05-13] (ang.).
- ↑ Kompostowane folie i torby [online] [dostęp 2009-05-13] [zarchiwizowane z adresu 2010-01-22] .
Bibliografia
- CRC Handbook of Chemistry and Physics, William M.W.M. Haynes (red.), wyd. 95, Boca Raton: CRC Press, 2014, ISBN 978-1-4822-0867-2 (ang.).
 Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
- p
- d
- e
- p
- d
- e
| G01A – Leki przeciwzakaźne i antyseptyczne (bez połączeń z kortykosteroidami) |
|
|---|
- p
- d
- e
- DSDE: mælkesyre