Kokaina
 | Ten artykuł należy dopracować: od 2010-04 → dodać przypisy do treści niemających odnośników do źródeł, → poprawić styl – powinien być encyklopedyczny. Dokładniejsze informacje o tym, co należy poprawić, być może znajdują się w dyskusji tego artykułu. Po wyeliminowaniu niedoskonałości należy usunąć szablon {{Dopracować}} z tego artykułu. |
| |||||||||||||||||||||||||||||||||||
 chlorowodorek kokainy | |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | C17H21NO4 | ||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa | 303,35 g/mol | ||||||||||||||||||||||||||||||||||
| Wygląd | biały krystaliczny proszek | ||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||
| Numer CAS | 50-36-2 | ||||||||||||||||||||||||||||||||||
| PubChem | 446220 | ||||||||||||||||||||||||||||||||||
| DrugBank | DB00907 | ||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||
| Klasyfikacja medyczna | |||||||||||||||||||||||||||||||||||
| ATC | N01BC01, R02AD03, S01HA01, S02DA02 | ||||||||||||||||||||||||||||||||||
| Legalność w Polsce | środek odurzający grupy I-N | ||||||||||||||||||||||||||||||||||
| Stosowanie w ciąży | kategoria C | ||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
Kokaina (łac. cocainum), pot. koks – organiczny związek chemiczny z grupy alkaloidów o szkielecie tropanu, ester metylowy benzoiloekgoniny. Ma właściwości pobudzające. Jest pozyskiwana z liści krasnodrzewu pospolitego (koki), który pierwotnie porastał tereny Andów w Ameryce Południowej. Odznacza się dużym potencjałem uzależniającym psychicznie[10].
Wykazuje podobieństwo strukturalne do kokatylenu i innych alkaloidów tropanowych, np. atropiny i skopolaminy.
- Porównanie budowy kokainy, kokatylenu, atropiny i skopolaminy
-
 kokaina
kokaina -
 kokatylen
kokatylen -
 atropina
atropina -
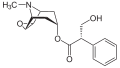 skopolamina
skopolamina
Historia
Kokaina to jeden z najstarszych i najniebezpieczniejszych stymulantów pochodzenia naturalnego[11]. Już 3000 lat p.n.e. starożytni Inkowie w Andach żuli liście koki. Przyspieszony oddech i bicie serca pomagało im w lepszym przystosowaniu się do życia wysokogórskiego, przeciwdziałając efektom rzadkiego powietrza na organizm.
Rdzenni Peruwiańczycy żuli liście koki tylko podczas ceremonii religijnych. Zmiana zaszła po najeździe Peru przez hiszpańskich żołnierzy w 1532 roku. Amerykanie-tubylcy, przymusowi robotnicy w hiszpańskich kopalniach srebra byli zaopatrywani w liście koki, ponieważ dzięki temu łatwiej było ich kontrolować i wykorzystywać.
Kokaina została po raz pierwszy wyizolowana z liści koki w 1859 roku przez niemieckiego chemika Alberta Niemanna. Dopiero w latach osiemdziesiątych XIX wieku zaczęto ją popularyzować w środowisku medycznym[12].
W późnych czasach wiktoriańskich używano kokainy dla rozrywki. Kokainę na szeroką skalę rozsławił Sigmund Freud, który był prawdziwym entuzjastą narkotyku. Stosował go regularnie przez wiele lat w małych dawkach jako środek przeciwko „depresji i niestrawności”[13].
W 1884 roku wiedeński okulista Karl Koller (1857-1944) umieścił roztwór kokainy na rogówce, uzyskując efekt znieczulający. Jego wyniki wzbudziły duże zainteresowanie i stały się początkiem współczesnych metod znieczulenia miejscowego[14][15][16]. Powierzchniowe użycie kokainy jest w dalszym ciągu stosowane w niektórych zabiegach okulistycznych i laryngologicznych[17].
Publikacje Freuda w czasopismach medycznych przedstawiające kokainę jako cudowne remedium na wszystkie dolegliwości sprawiły, że zaczęto ją sprzedawać na dużą skalę bez recepty w aptekach i drogeriach. Używano jej w różnych medykamentach, lekarstwach na ból zębów, papierosach i różnorodnych napojach, zarówno bezalkoholowych, jak i w winie. Dostępne były także preparaty przeznaczone dla dzieci[18]. W przypadku przyjmowania kokainy z alkoholem jest ona przekształcana w wątrobie w kokatylen o dłuższym czasie działania[19]. Było to przyczyną popularności domieszkowania win kokainą (najbardziej znane było Vin Mariani[18]). Wina kokainowe zyskały sobie smakoszy wśród premierów, szlachty, a nawet papieży. Architekt Frédéric-Auguste Bartholdi stwierdził, że gdyby posmakował Vin Mariani wcześniej, zaprojektowałby Statuę Wolności o kilkaset metrów wyższą.
Napój Coca-cola wszedł na rynek w 1886 roku jako mieszanka ekstraktów liści krzewu koka i nasion drzewa kola. Reklamowano ją jako „wartościowy napój pobudzający umysł i leczący wszystkie przypadłości nerwowe”. Do 1903 r. typowe opakowanie zawierało około 60 mg kokainy. Dzisiejsza Coca-cola nadal zawiera ekstrakt z liści koki – The Coca-Cola Company importuje obecnie ok. 8 ton liści rocznie, jednak zabieg ten ma wpływ jedynie na walory smakowe, gdyż narkotyk jest usuwany.
W handlu dostępne były tabletki Forced March, zawierające mieszaninę kokainy i kofeiny. Korzystali z nich (obok innych narkotyków[20]) m.in. polarnicy Ernest Shackleton i Robert Scott podczas ekspedycji na biegun południowy, a także żołnierze podczas I wojny światowej[21].
Opowiadanie Roberta Stevensona Doktor Jekyll i pan Hyde, opublikowane w 1886 roku, powstało podczas sześciodniowej sesji kokainowej. Fikcyjna postać literacka, która po raz pierwszy pojawiła się w powieści wydanej w 1887, bohater znanych opowiadań detektywistycznych Artura Conana Doyle’a – Sherlock Holmes – nie stronił od przyjmowania kokainy dożylnie.
W 1886 r. nastąpił wzrost doniesień z całego świata o nowych przypadkach kokainizmu i ostrych zatruciach kokainą[potrzebny przypis]. W rezultacie część osób przestała zażywać kokainę, inni przerzucili się z zastrzyków na przyjmowanie doustne jako rzekomo mniej szkodliwe. Rozpowszechnienie Coca-Coli wspierało ten proces. Używanie kokainy stawało się wówczas modne w pewnych kręgach, takich jak artyści, intelektualiści, pisarze oraz gangsterzy.
Po pierwszej wojnie światowej kokaina została w większości państw zakazana. Jednak nadal była popularna, choć na zmniejszenie jej popularności wpłynęło pojawienie się heroiny.
Popularność kokainy zwiększyła się ponownie w USA w latach 70 dwudziestego wieku i zaczęła wypierać marihuanę. W dystrybucji narkotyku dostrzegli interes Kolumbijczycy: bracia Fabio Ochoa, Jorge Ochoa i Juan David Ochoa oraz Pablo Escobar, którzy stworzyli kartel narkotykowy z Medellin.
W 1996 r. gazeta San Jose Mercury News opublikowała serię artykułów śledczych pt. Ciemny związek (Dark Alliance), zarzucając spowodowanie epidemii kokainizmu w gettach amerykańskich świadomym i celowym działaniom CIA. Publikacja wywołała oburzenie społeczne w USA[potrzebny przypis], aczkolwiek nie pociągnięto ważnych osób do odpowiedzialności karnej.
Synteza
Badania nad syntezą kokainy zapoczątkował Carl Liebermann. Wówczas jednak nie była znana metoda otrzymania tropinonu (proponowanego substratu), przez co nie zostały opracowane warunki syntezy. Tropinon z cykloheptanonu otrzymał po raz pierwszy Richard Willstätter, jednak wydajność zaproponowanej reakcji była mała i nie pozwoliła na dobranie warunków syntezy samej kokainy[22][23]. Dopiero po opracowaniu prostej i wydajnej metody syntezy tropinonu przez Roberta Robinsona w roku 1917[24] Willstätter opracowywał warunki syntezy i w 1923 otrzymał syntetyczną kokainę[25].
Kokaina w medycynie
W laryngologii i okulistyce stosuje się 1–20% roztwór chlorowodorku kokainy w celu znieczulenia miejscowego ze względu na efekt sympatykomimetyczny, dzięki któremu dochodzi do obkurczenia naczyń błony śluzowej zmniejszając przy tym krwawienie, lub rozszerzenia źrenicy ułatwiającego prowadzenie wielu zabiegów na oku. Mechanizm tego działania związany jest ze zmniejszeniem przepuszczalności błony komórkowej w stosunku do jonów sodu, co hamuje proces depolaryzacji, w efekcie czego tworzy się lokalny blok przewodzenia impulsów nerwowych[17]. Dawka jednorazowa nie może przekraczać 30 mg, a dobowa – 60 mg[26]. W Polsce nie znajduje się w urzędowym wykazie leków dopuszczonych do obrotu[27].
Działanie ogólnoustrojowe
- Hamuje wychwyt zwrotny noradrenaliny przez neurony ośrodkowego i obwodowego układu nerwowego. Powoduje to:
- silny skurcz naczyń krwionośnych i wzrost ciśnienia tętniczego
- rozszerzenie źrenic
- rozkurcz mięśniówki oskrzeli
- zahamowanie perystaltyki przewodu pokarmowego
- zahamowanie wydzielania śliny przez gruczoły ślinowe.
- Hamuje wychwyt zwrotny dopaminy, co powoduje:
- w mniejszych dawkach – pobudzenie psychoruchowe, uczucie euforii, omamy
- w większych – depresja ośrodka oddechowego w pniu mózgu.
- pobudzenie receptorów β na obwodzie, co wywołuje:
- dodatni efekt chronotropowy, dromotropowy i inotropowy na serce, a co za tym idzie, wzrost ciśnienia tętniczego i zaburzenia rytmu serca, prowadzące do takich chorób jak:
- nadczynność tarczycy.
Narkotyk
Produkcja
Ponad połowa światowej produkcji kokainy odbywa się w Kolumbii. Rolnicy po zebraniu liści krasnodrzewu pospolitego siekają je drobno i polewają ciekłym nawozem dla zmiękczenia liści. Liście przygotowane w ten sposób wrzucane są do beczek i zalewane benzyną (rozpuszczalnik) w celu wyekstrahowania substancji psychoaktywnej (zawartość substancji psychoaktywnej w liściach wynosi do 2%)[28]. Następnie liście usuwane są z mieszaniny, która zostaje zneutralizowana sodą oczyszczoną. Powstałą mieszankę podgrzewa się by odparować ciecz, a pozostałą pastę się suszy. Kolumbijscy rolnicy produkujący pastę kokainową sprzedają ją przestępcom. Otrzymują za to niewielkie wynagrodzenie w stosunku do wartości produktu kupionego przez narkomana. Szacuje się, że z każdego grama kokainy sprzedanego na ulicy rolnik otrzymuje 0.05 USD[29].
Lewamizol bywa dodawany do kokainy sprzedawanej w Stanach Zjednoczonych Ameryki ze względu na niższą cenę i podobne oddziaływanie. Dodatek powoduje u zażywających plamicę i zmniejszenie ilości neutrofili[30].
Sól kokainy

Kokaina w postaci soli - np. chlorowodorku to śnieżnobiały lub żółtawy proszek. Przed wprowadzeniem na rynek jest mieszana z innymi substancjami (wypełniaczami), w celu zwiększenia objętości. Substancje używane w tym procesie to soda oczyszczona, cukry np. laktoza, glukoza, poliole np. inozytol, mannitol i środki znieczulające miejscowe, np. lidokaina. Ta postać kokainy jest rozpuszczalna w wodzie, dzięki czemu można ją wypić lub wstrzyknąć.
Kokaina jako tzw. wolna zasada
Sól kokainy można przekształcić w tak zwaną wolną zasadę, aminę (czyli kokaina, nie jej sól) poprzez zalkalizowanie jej roztworu, a następnie ekstrakcję kokainy za pomocą rozpuszczalnika organicznego. Procedura usuwa niektóre zanieczyszczenia z produktu w formie proszku i wielu zażywających kokainę uważa ją za mniej szkodliwą formę narkotyku.
Krak (crack)

Nazwa krak pochodzi od ang. crack (pękanie), ze względu na dźwięki powstające podczas jego palenia. To kokaina w formie wolnej zasady, wyizolowana przez strącanie podczas gotowania roztworu chlorowodorku kokainy i sody oczyszczonej.
W porównaniu z innymi formami kokainy krak jest silnie uzależniający, o natychmiastowym, krótkotrwałym działaniu (5 do 10 minut). Narkotyk jest zażywany poprzez podgrzewanie i wdychanie oparów. Crack pojawił się w USA w latach osiemdziesiątych XX wieku.
Ogólnie opisując, narkotyk uliczny zawiera różne stężenia kokainy w mieszaninie, zależnie od dedykowanego klienta, rzadkie ok. 90%, powszechnie 40 do 60%.
Zażywanie kokainy
Postać i sposób zażywania kokainy wpływa na intensywność i czas efektów narkotycznych, a także na szybkość powstawania uzależnienia. Intensywność efektu zależy od ilości narkotyku jaka dostała się z krwią do mózgu. Procent zaabsorbowanego narkotyku zależy również od przyjętej dawki. Im większa, tym mocniejsze i dłuższe działanie.
Im szybciej narkotyk dostaje się do mózgu, tym szybciej odczuwalne są efekty działania. Długość i intensywność wiąże się z metodą podania narkotyku. Efekt odurzenia odczuwalny jest niedługo po zażyciu kokainy. Odczucia psychotropowe, określane jako high, są powiązane ze stężeniem narkotyku we krwi. Im szybciej kokaina dotrze do mózgu, tym większe będą efekty; szybciej również znikną. Sposób przyjmowania kokainy ma wpływ na odczucia. Metoda powodująca szybkie i intensywne odczucia, daje odurzenie trwające krócej.

Główne metody wprowadzenia kokainy do organizmu:
Żucie
- Żuje się listki koki, które zazwyczaj wymieszane są z substancją o charakterze zasadowym (np. wapnem), lub parzy się je jak herbatę i pije.
Wciąganie
- Nosem Wdychana nosem sproszkowana kokaina dostaje się do krwiobiegu poprzez śluzówkę.
- Ustami tzw. po kolumbijsku. Polega na bezpośrednim wdychaniu sproszkowanej kokainy za pomocą długiej cienkiej rurki, efekty po zażyciu są podobne jak przy wciągnięciu nosem.
Wstrzykiwanie
- wprowadzenie rozpuszczonej kokainy bezpośrednio w krwiobieg. W ten sposób narkotyk w całości dostaje się do krwiobiegu z pominięciem naturalnych systemów obronnych organizmu. Stwarza to zagrożenie przedawkowania w krótkim czasie. Tak podanej kokainie dotarcie do mózgu zabiera około jednej minuty. Czas potrzebny do osiągnięcia maksymalnych efektów psychotropowych i fizjologicznych jest krótszy niż w przypadku innych metod. Maksymalny efekt fizjologiczny pojawia się po dziesięciu minutach, a psychotropowy po czterech minutach. Oba trwają po około trzynaście minut.
Palenie
- Wdychanie oparów kokainy (wolna zasada, crack) lub dymu do płuc. Inhalacja sprawia, że kokaina dostaje się do mózgu po 19 sekundach, jakkolwiek tylko 30–60% dawki zostaje wchłonięte. Opary wdycha się przez odpowiednio skonstruowaną fajkę. Palacze osiągają maksymalny efekt fizjologiczny po dwóch minutach, a psychotropowy po jednej minucie. Efekty utrzymują się krótko – od 10 do 30 minut[potrzebny przypis].
Efekty psychotropowe
Na siłę efektów wpływa ilość przyjętej dawki. Kokaina wpływa dodatnio na poziom dopaminy – odpowiedzialnej za układ nagrody w mózgu. Powoduje odczucie euforii, zmniejsza niepokój i zwiększa poczucie pewności siebie, zwłaszcza w kontaktach międzyludzkich. Duże dawki kokainy, wprowadzone którymś z wydajnych sposobów do organizmu, powodują euforyczne doświadczenia, tworzące jaskrawe, długoterminowe wspomnienia, stanowiące podstawę dla później pojawiającej się ochoty na narkotyk. Przy większych dawkach powstają również halucynacje i paranoje, przypominające objawy schizofrenii.
Właściwości uzależniające
Kokaina bardzo silnie uzależnia psychicznie, powodując zmiany w mózgu[31].
Po zażyciu kokainy następuje okres euforii, a potem okres złego samopoczucia, który skłania do zażycia kolejnej dawki. Przyjemne efekty wywoływane przez kokainę są przyczyną powstania wewnętrznego przymusu ciągłego używania narkotyku pomimo niekorzystnych skutków, jakie mogą wystąpić. To łaknienie jest spowodowane uzależnieniem psychicznym. Powoduje ciągłe zwiększanie dawek.
Inne niebezpieczeństwa
Efekty wymienione poniżej nie są widoczne po pierwszym, drugim zażyciu narkotyku, jednak nasilają się z każdą kolejną dawką.
- zaburzenia osobowości
- depresja z próbami samobójczymi
- psychoza pokokainowa – zaburzenia funkcjonowania społecznego i urojenia, w tym urojenia prześladowcze
- krwawienia z nosa
- zniszczenie błony śluzowej
- przedziurawienie przegrody nosowej
- aseptyczna martwica przegrody nosowej
- kaszel
- chrypka
- duszność
- trudności z donoszeniem ciąży
- zwiększona umieralność noworodków u matek używających kokainę
Do ww. objawów trzeba dodać objawy wynikające z zachowania podczas odurzenia – urazy, samobójstwa, zabójstwa.
Przedawkowanie
Ostre zatrucie zazwyczaj występuje po przyjęciu sproszkowanej kokainy w ilości 500 mg[17]. Natomiast wstrzyknięcie już 20 mg dożylnie kończy się śmiercią spowodowaną porażeniem ośrodka oddechowego (śmierć przez uduszenie)[potrzebny przypis]. Zanim to nastąpi, mają miejsce następujące objawy zatrucia ostrego:
- drgawki,
- podwyższone ciśnienie krwi, kołatanie serca (przyśpieszone i niemiarowe bicie serca),
- zablokowanie ośrodka oddechowego zlokalizowanego w mózgu,
- napady szału z jednoczesnym zamroczeniem.
Po pewnym czasie może pojawić się znużenie, senność, a w końcu traci się świadomość, co sprzyja ustaniu czynności oddechowej.
Zewnętrzne oznaki używania
Do zewnętrznych objawów zażycia kokainy należą:
- nadpobudliwość i wzmożona aktywność,
- pobudzenie seksualne,
- zwiększona rozmowność, towarzyskość i pewność siebie,
- rozszerzone źrenice, słabo reagujące na światło.
- katar
Zobacz też
- speedball
Przypisy
- ↑ Farmakopea Polska VI, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2002, s. 1176, ISBN 83-88157-18-3 .
- ↑ a b c d e CRC Handbook of Chemistry and Physics, William M.W.M. Haynes (red.), wyd. 97, Boca Raton: CRC Press, 2016, s. 3-126, 5145, ISBN 978-1-4987-5429-3 (ang.).
- ↑ Kokaina, wolna zasada (nr C8912) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. [dostęp 2020-01-03]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ a b c d Cocaine, [w:] ChemIDplus, United States National Library of Medicine [dostęp 2020-01-03] (ang.).
- ↑ Kokaina (nr C8912) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2011-06-24]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ K.K. Fattinger K.K. i inni, Nasal mucosal versus gastrointestinal absorption of nasally administered cocaine, „European Journal of Clinical Pharmacology”, 56 (4), 2000, s. 305–310, DOI: 10.1007/s002280000147, PMID: 10954344 .
- ↑ GeneG. Barnett GeneG., RichardR. Hawks RichardR., RichardR. Resnick RichardR., Cocaine pharmacokinetics in humans, „Journal of Ethnopharmacology”, 3 (2–3), 1981, s. 353–366, DOI: 10.1016/0378-8741(81)90063-5, PMID: 7242115 .
- ↑ A.R.A.R. Jeffcoat A.R.A.R. i inni, Cocaine disposition in humans after intravenous injection, nasal insufflation (snorting), or smoking, „Drug Metabolism and Disposition”, 17 (2), 1989, s. 153–159, PMID: 2565204 .
- ↑ a b Cocaine, [w:] DrugBank, University of Alberta, DB00907 (ang.).
- ↑ American Addiction Centers EditorialA.A.C.E. Staff American Addiction Centers EditorialA.A.C.E., Cocaine Addiction: Statistics, Side Effects, Risks & Treatment [online], luxury.rehabs.com [dostęp 2021-03-15] (ang.).
- ↑ MichaelM. Gossop MichaelM., Classification of illegal and harmful drugs, „BMJ : British Medical Journal”, 333 (7562), 2006, s. 272–273, DOI: 10.1136/bmj.38929.578414.80, ISSN 0959-8138, PMID: 16888294, PMCID: PMC1526938 [dostęp 2021-03-15] .
- ↑ Cocaine: A short history [online], Foundation for a drug-free world [dostęp 2020-10-12] .
- ↑ Henry L.H.L. Lennard Henry L.H.L., Freud's Disaster With Cocaine, „The New York Times”, 22 lipca 1972 .
- ↑ MichaelM. Goerig MichaelM., DouglasD. Bacon DouglasD., André vanA. Zundert André vanA., Carl Koller, cocaine, and local anesthesia: some less known and forgotten facts, „Regional Anesthesia and Pain Medicine”, 37 (3), 2012, s. 318–324, DOI: 10.1097/AAP.0b013e31825051f3, PMID: 22531385 [dostęp 2021-03-16] (ang.).
- ↑ H.H. Honegger H.H., H.H. Hessler H.H., Die Entdeckung der Lokalanasthesie durch Karl Koller. I, „Klinische Monatsblatter Fur Augenheilkunde”, 157 (3), 1970, s. 428–438, PMID: 4922411 [dostęp 2021-03-16] (niem.).
- ↑ Karl Koller, local anaesthesia and cocaine [online], cocaine.org [dostęp 2021-03-16] .
- ↑ a b c WojciechW. Kostowski WojciechW., Zbigniew S.Z.S. Herman Zbigniew S.Z.S., Farmakologia. Podstawy farmakoterapii. Podręcznik dla studentów medycyny i lekarzy, wyd. 3, Warszawa: Wydawnictwo Lekarskie PZWL, 2006, s. 1569, ISBN 83-200-3352-7 .
- ↑ a b 11 Unbelievable Moments from Cocaine’s Early Medical History [online], Mental Floss [dostęp 2020-10-13] (ang.).
- ↑ P.P. Jatlow P.P. i inni, Alcohol plus cocaine: the whole is more than the sum of its parts, „Therapeutic Drug Monitoring”, 18 (4), 1996, s. 460–464, DOI: 10.1097/00007691-199608000-00026, PMID: 8857569 (ang.).
- ↑ MariaM. Godoy MariaM., 'Cocaine For Snowblindness': What Polar Explorers Packed For First Aid [online], NPR.org, 28 września 2012 [dostęp 2020-10-13] (ang.).
- ↑ JoannaJ. Bourke JoannaJ., Enjoying the high life—drugs in history and culture, „The Lancet”, 376 (9755), 2010, s. 1817, DOI: 10.1016/S0140-6736(10)62153-8, PMID: 24910482, PMCID: PMC4046111 (ang.).
- ↑ Organic Synthesis, Cambridge: Royal Society of Chemistry, 1998, DOI: 10.1039/9781847551573, ISBN 978-0-85404-544-0 (ang.).
- ↑ RichardR. Willstätter RichardR., AdolfA. Bode AdolfA., Synthese von r-Cocaïn, „Justus Liebig’s Annalen der Chemie”, 326 (1–2), 1903, s. 42–78, DOI: 10.1002/jlac.19033260104 (niem.).
- ↑ Investigating a scientific legend: the tropinone synthesis of Sir Robert Robinson, F. R. S, „Notes and Records of the Royal Society of London”, 47 (2), 1993, s. 277–296, DOI: 10.1098/rsnr.1993.0034 (ang.).
- ↑ Organic reactions, Hoboken: Wiley Online Library, 2003–, ISBN 978-0-471-26418-7, OCLC 351199560 .
- ↑ Farmakopea Polska VIII, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2008, s. 3491, ISBN 978-83-88157-53-0 .
- ↑ Obwieszczenie Prezesa Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych z dnia 31 marca 2011 r. w sprawie ogłoszenia Urzędowego Wykazu Produktów Leczniczych Dopuszczonych do Obrotu na terytorium Rzeczypospolitej Polskiej [online] [dostęp 2011-12-28] [zarchiwizowane z adresu 2011-10-27] (pol.).
- ↑ J.K.J.K. Piotrowski J.K.J.K., Podstawy toksykologii, Warszawa: Wydawnictwa Naukowo-Techniczne, 2006, s. 492, ISBN 83-204-3122-0 .
- ↑ National Geographic – serial dokumentalny (Drugs Inc.: Cocaine).
- ↑ FrancieF. Diep FrancieF., Kokaina coraz groźniejsza, „Świat Nauki”, 10 (242), Prószyński Media, październik 2011, s. 12, ISSN 0867-6380 .
- ↑ N.D.N.D. Volkow N.D.N.D. i inni, Changes in brain glucose metabolism in cocaine dependence and withdrawal, „The American Journal of Psychiatry”, 148 (5), 1991, s. 621–626, DOI: 10.1176/ajp.148.5.621, PMID: 2018164 .
Linki zewnętrzne
- „Sigmund Freud – psychoanaliza, sny, popędy seksualne, kokaina”, 14.08.2020, Portal SiedemÓsmych
- Materiały dokumentalnego filmu o narkotykach w USA
- Stanisław Ignacy Witkiewicz – Nikotyna, Alkohol, Kokaina etc... Doświadczenia własne
 Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
- p
- d
- e
- p
- d
- e
| N01A – Leki do znieczulenia ogólnego |
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| N01B – Środki do znieczulenia miejscowego |
|
- p
- d
- e
| R02AA – Środki antyseptyczne |
|
|---|---|
| R02AB – Antybiotyki |
|
| R02AD – Środki miejscowo znieczulające |
|
| R02AX – Inne |
- p
- d
- e
| S01A – Leki stosowane w zakażeniach oczu |
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| S01B – Leki przeciwzapalne |
| ||||||||||||
| S01C – Połączenia leków przeciwzapalnych z przeciwinfekcyjnymi |
| ||||||||||||
| S01E – Leki stosowane w jaskrze i zwężające źrenicę |
| ||||||||||||
| S01F – Leki rozszerzające źrenicę |
| ||||||||||||
| S01G – Leki zmniejszające przekrwienie oraz przeciwalergiczne |
| ||||||||||||
| S01H – Środki znieczulające miejscowo |
| ||||||||||||
| S01J – Preparaty diagnostyczne |
| ||||||||||||
| S01K – Preparaty pomocnicze w chirurgii oka |
| ||||||||||||
| S01L – Leki stosowane w leczeniu zaburzeń naczyniowych oka |
| ||||||||||||
| S01X – Pozostałe leki oftalmologiczne |
|
- p
- d
- e
| S02A – Leki przeciwinfekcyjne |
| ||
|---|---|---|---|
| S02B – Kortykosteroidy |
| ||
| S02C – Połączenia kortykosteroidów i leków przeciwinfekcyjnych |
| ||
| S02D – Inne leki otologiczne |
|
- p
- d
- e
| Adamantany (pochodne adamantanu) |
|
|---|---|
| Antagonisty adenozyny |
|
| Alkiloaminy |
|
| Ampakiny |
|
| Arylocykloheksyloaminy |
|
| Benzoazepiny |
|
| Cholinergiki |
|
| Konwulsanty |
|
| Eugeroiki | |
| Oksazoliny |
|
| Fenyloetyloaminy |
|
| Fenylomorfoliny |
|
| Piperazyny | |
| Piperydyny |
|
| Pirolidyny |
|
| Racetamy |
|
| Tropany |
|
| Tryptaminy |
|
| Inne |
|
- Britannica: science/cocaine
- Treccani: cocaina
- Universalis: cocaine
- БРЭ: 2079205
- DSDE: kokain





















